 发病机制
发病机制
发病机制:发病机制尚未完全阐明。基因研究的成果为揭示本病的发病机制提出了新的见解。正常人集合管上皮细胞管腔膜上钠通道蛋白由α、β、γ 三种亚基构成。由于基因突变,患者集合管上皮细胞管腔膜上通道蛋白的富含脯氨酸的β亚单位及γ亚单位在与细胞骨架蛋白的相互作用下,发生构象改变,使通道蛋
白发生构象性活化,导致Na
的再吸收显著增加,血容量扩张。同时该通道蛋白又缺乏降调节(down regulation)作用,相应地对低肾素性高血压也缺乏降调节。由于持久性的Na
再吸收增加导致排K
、泌H
增多,产生高血压、低血钾、碱中毒以及低肾素性
低醛固酮血症。
另外,在钠通道蛋白的活性调节中,通道蛋白的多形性也起着重要作用。
据Braro等人观察,限制钠盐可使皮质酮分泌增加,而醛固酮仍低于正常,提示由皮质酮向醛固酮合成可能有阻滞。现认为利德尔综合征可能反映全身钠转运异常,Helbook和Reynolds发现患者红细胞钠内流增加,导致细胞内高压。给患者氨苯蝶啶同时限制钠摄入,结果红细胞对钠的吸收减少,细胞内钠浓度减低。但尽管细胞内钠浓度正常,红细胞离子流入和溢出分数仍增加,将红细胞放在肾素-醛固酮含量都正常的血浆中孵育亦不能改变此结果。患者的唾液和汗液钠钾比例增高,故认为肾小管细胞亦有这种变化,即细胞内高钠刺激远曲小管泌钾和保钠,钠潴留又抑制了肾素-醛固酮系统的功能,从而引起本病一系列症状的发生。
 临床表现
临床表现
临床表现:临床症状与原发性醛固酮增多症相似,主要是高血压、低血钾与碱中毒。病人表现为
头痛、肌肉无力及软瘫、多尿、烦渴、抽搐、感觉异常、视网膜病变。与原发性醛固酮增多症不同的是血及尿中醛固酮含量不高。化验检查呈严重肾性失钾,血钾常低至2.4~3.5mmol/L,而血醛固酮不高或降低,尿17-羟和17酮类固醇及ATCH试验均正常;血醛固酮低可能是由于低血钾、高血容量或高血压的原因。另外,患者唾液及汗液中Na
与K
比值检测正常或稍高,粪钾正常;本病服用螺内酯无效,对氨苯蝶啶或限盐治疗有效,如给予肾小管潴钾利尿药氨苯蝶啶及补充氯化钾可使血压恢复正常。
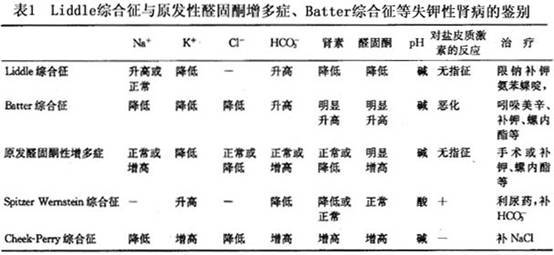
本病应与原发性醛固酮增多症及Bartter综合征等失钾性疾病相鉴别。高血压、低血钾与原发性醛固酮增多症有相似之处,但是本病呈
低醛固酮血症,对螺内酯治疗无效,唾液及汗液Na
/K
比例增高可资鉴别。Bartter综合征虽有低血钾、碱中毒但血压正常,血及尿中醛固酮含量增高,血浆肾素活性及血管肾张素也增高,肾活检可见肾小球旁器增生。11β-羟脱氢酶缺乏症可表现为高血压、低血钾碱中毒与生长发育障碍。但尿17羟及17酮升高,尿四羟皮质醇亦升高,可以鉴别。
 治疗
治疗
治疗:本病的治疗原则是限制钠盐摄入,适当补充钾盐,一般每天给予
氯化钾3.0g即可。氨苯蝶啶抑制远曲小管离子转运,使钠排泄增加,钾排泄减少,剂量每天8~10mg/kg,口服3个月可纠正电解质紊乱,综合以上治疗可纠正血和尿电解质变化并使血压降低。具体方法如下:
1.补充
氯化钾 临床常主张口服或注射补充门冬酰氨钾镁,在补钾的同时需注意预防低血镁。在严重低血钾引起的肌麻痹及严重心律失常时,则可短暂加以补充
氯化钾,待血钾升至正常水平后即停止补钾,以免发生高钾血症。对血钾、血钙已恢复正常,但仍有低血镁、伴神经肌肉应激性增强和(或)频发性心脏期前收缩者,经静注钙剂无效时,可给镁剂纠正。通过肾小管排钠潴钾,可使患者血钾迅速升高,代谢性碱中毒消失,并使血压、
血浆肾素活性及醛固酮恢复正常。
2.保钾利尿 口服氨苯蝶啶和阿米洛利(氨氯吡咪),剂量为氨苯蝶啶50~100g/次,2~3/d。该病应终身服用氨苯蝶啶或阿米洛利(氨氯吡咪)方能维持健康状态。在用药过程中,需定期监测血钾、钠、氯和CO2CP,及时调整剂量,以免发生高血钾、低血钠和高血氯性酸中毒。
3.低钠饮食 在应用氨苯喋啶或阿米洛利(氨氯吡咪)时,必须十分强调应同时给予低钠饮食的重要性。每天饮食中最多给予2g
氯化钠粉剂。采取低钠饮食的方法,也可以扭转电解质紊乱和防止高血压发生。



 流行病学
流行病学
 病因
病因
 发病机制
发病机制
 临床表现
临床表现
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后
 预防
预防